- SOLUCIONES QUÍMICAS
Una solución es una mezcla homogénea de dos o más sustancias. La sustancia disuelta se denomina soluto y está presente generalmente en pequeña cantidad en pequeña cantidad en comparación con la sustancia donde se disuelve denominada solvente. en cualquier discusión de soluciones, el primer requisito consiste en poder especificar sus composiciones, esto es las cantidades relativas de los diversos componentes.
La concentración de una solución expresa la relación de la cantidad de soluto a la cantidad de solvente.
Las soluciones poseen una serie de propiedades que las caracterizan:
1. | Su composición química es variable. | |
2. | Las propiedades químicas de los componentes de una solución no se alteran. | |
Las propiedades físicas de la solución son diferentes a las del solvente puro: la adición de un soluto a un solvente aumenta su punto de ebullición y disminuye su punto de congelación; la adición de un soluto a un solvente disminuye la presión de vapor de éste. | ||
PRINCIPALES CLASES DE SOLUCIONES
SOLUCIÓN | DISOLVENTE | SOLUTO | EJEMPLOS |
Gaseosa | Gas | Gas | Aire |
Liquida | Liquido | Liquido | Alcohol en agua |
Liquida | Liquido | Gas | O2 en H2O |
Liquida | Liquido | Sólido | NaCl en H2O |
SOLUBILIDAD
La solubilidad es la cantidad máxima de un soluto que puede disolverse en una cantidad dada de solvente a una determinada temperatura
Factores que afectan la solubilidad:
Los factores que afectan la solubilidad son:
a) Superficie de contacto: La interacción soluto-solvente aumenta cuando hay mayor superficie de contacto y el cuerpo se disuelve con más rapidez ( pulverizando el soluto).
b) Agitación: Al agitar la solución se van separando las capas de disolución que se forman del soluto y nuevas moléculas del solvente continúan la disolución
c) Temperatura: Al aument6ar la temperatura se favorece el movimiento de las moléculas y hace que la energía de las partículas del sólido sea alta y puedan abandonar su superficie disolviéndose.
d) Presión: Esta influye en la solubilidad de gases y es directamente proporcional
MODO DE EXPRESAR LAS CONCENTRACIONES
MODO DE EXPRESAR LAS CONCENTRACIONES
La concentración de las soluciones es la cantidad de soluto contenido en una cantidad determinada de solvente o solución. Los términos diluida o concentrada expresan concentraciones relativas. Para expresar con exactitud la concentración de las soluciones se usan sistemas como los siguientes:
a) Porcentaje peso a peso (% P/P): indica el peso de soluto por cada 100 unidades de peso de la solución.
b) Porcentaje volumen a volumen (% V/V): se refiere al volumen de soluto por cada 100 unidades de volumen de la solución.
c) Porcentaje peso a volumen (% P/V): indica el número de gramos de soluto que hay en cada 100 ml de solución.
d) Fracción molar (Xi): se define como la relación entre las moles de un componente y las moles totales presentes en la solución.
e) Molaridad ( M ): Es el número de moles de soluto contenido en un litro de solución. Una solución 3 molar ( 3 M ) es aquella que contiene tres moles de soluto por litro de solución.
f) Molalidad (m): Es el número de moles de soluto contenidos en un kilogramo de solvente. Una solución formada por 36.5 g de ácido clorhídrico, HCl , y 1000 g de agua es una solución 1 molal (1 m)
g) Normalidad (N): Es el número de equivalentes gramo de soluto contenidos en un litro de solución.
h) Formalidad (F): Es el cociente entre el número de pesos fórmula gramo (pfg) de soluto que hay por cada litro de solución. Peso fórmula gramo es sinónimo de peso molecular. La molaridad (M) y la formalidad (F) de una solución son numéricamente iguales, pero la unidad formalidad suele preferirse cuando el soluto no tiene un peso molecular definido, ejemplo: en los sólidos iónicos.
SOLUCIONES DE ELECTROLITOS
SOLUCIONES DE ELECTROLITOS
Electrolitos:
Son sustancias que confieren a una solución la capacidad de conducir la corriente eléctrica. Las sustancias buenas conductoras de la electricidad se llaman electrolitos fuertes y las que conducen la electricidad en mínima cantidad son electrolitos débiles.
Electrolisis:
Son las transformaciones químicas que producen la corriente eléctrica a su paso por las soluciones de electrolitos.
Al pasar la corriente eléctrica, las sales, los ácidos y las bases se ionizan.
Fuente: http://www.cespro.com/Materias/MatContenidos/Contquimica/QUIMICA_INORGANICA/soluciones.htm.
- EL PH

El pH es una medida de la acidez o alcalinidad de una solución. El pH indica la concentración de iones hidronio [H3O+] presentes en determinadas sustancias. La sigla significa "potencial de hidrógeno" (pondus Hydrogenii o potentia Hydrogenii; del latín pondus, n. = peso; potentia, f. = potencia; hydrogenium, n. = hidrógeno). Este término fue acuñado por el químico danés Sørensen, quien lo definió como el logaritmo negativo de base 10 de la actividad de los iones hidrógeno. Esto es:
Desde entonces, el término "pH" se ha utilizado universalmente por lo práctico que resulta para evitar el manejo de cifras largas y complejas. En disoluciones diluidas, en lugar de utilizar la actividad del ion hidrógeno, se le puede aproximar empleando la concentración molar del ion hidrógeno.
pH = - log 10 [aH3O+]
Desde entonces, el término "pH" se ha utilizado universalmente por lo práctico que resulta para evitar el manejo de cifras largas y complejas. En disoluciones diluidas, en lugar de utilizar la actividad del ion hidrógeno, se le puede aproximar empleando la concentración molar del ion hidrógeno.
Por ejemplo, una concentración de [H3O+] = 1 × 10–7 M (0,0000001) es simplemente un pH de 7 ya que: pH = –log[10–7] = 7
El pH típicamente va de 0 a 14 en disolución acuosa, siendo ácidas las disoluciones con pH menores a 7 (el valor del exponente de la concentración es mayor, porque hay más protones en la disolución) , y alcalinas las que tienen pH mayores a 7. El pH = 7 indica la neutralidad de la disolución (donde el disolvente es agua).
Se considera que p es un operador logarítmico sobre la concentración de una solución: p = –log[...] , también se define el pOH, que mide la concentración de iones OH−.
Puesto que el agua está disociada en una pequeña extensión en iones OH– y H3O+, tenemos que:
K(constante)w(water; agua) = [H3O+]·[OH–]=10–14 en donde [H3O+] es la concentración de iones hidronio, [OH−] la de iones hidroxilo, y Kw es una constante conocida como producto iónico del agua, que vale 10−14.
Por lo tanto,
log Kw = log [H3O+] + log [OH–]
–14 = log [H3O+] + log [OH–]
14 = –log [H3O+] – log [OH–]
pH + pOH = 14
Por lo que se puede relacionar directamente el valor del pH con el del pOH.
En disoluciones no acuosas, o fuera de condiciones normales de presión y temperatura, un pH de 7 puede no ser el neutro. El pH al cual la disolución es neutra estará relacionado con la constante de disociación del disolvente en el que se trabaje.
- CLASIFICACIÓN DE LAS ESPECIES
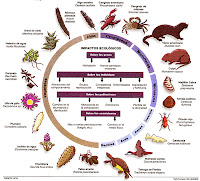
Especie: es el conjunto de organismos que pueden reproducirse entre sí y dar lugar a descendentes que también son fértiles.
Biodiversidad: el conjunto de especies que viven o han vivido en la Tierra. Una forma de medir la biodiversidad de una zona es calculando la probabilidad que al coger dos organismos al azar sean de especies diferentes. Si esta probabilidad es alta se dice que la biodiversidad de la zona es alta. Es el que pasa por ejemplo en un arrecife coralino y en una selva virgen. Si esta probabilidad es baja, se dice que la biodiversidad de la zona es baja. Es el que pasa por ejemplo en un campo de trigo o en un hormiguero.
Historia de las clasificaciones de los organismos.
El elevado número de especies descubiertas ha hecho necesario agruparlas para facilitar su estudio. Por ejemplo para averiguar si un individuo es de una especie o de otra muy parecida, conviene que todas las especies parecidas se agrupen juntas.
Las principales clasificaciones propuestas a lo largo de la historia son:
1. La clasificación de Aristóteles: Hace más de 2000 años este filósofo griego pensaba que sólo había unos cuantos centenares de especies. Las clasificó en dos reinos: el Reino de los animales y el Reino de las plantas. Además, los animales se dividían en dos grupos según si tenían o no sangre roja.
2. La clasificación de Linné: Linné fue un gran botánico sueco que vivió entre 1707 y 1778. Estableció una jerarquía de grupos llamados taxones. En ella, cada grupo de nivel superior abarca un o varios grupos de nivel inferior. También ideó la nomenclatura binomial de las especies que se explica más abajo.
• Taxón: Se denomina taxón a cualquier grupo de organismos dentro de una clasificación jerarquizada de seres vivos.
• Tipos de taxones: De orden superior a inferior son: Reino, filum, clase, orden, familia, genero, especie.
Un Reino abarca varios Fílums, un Fílum abarca varias Clases y así sucesivamente.
• Taxonomía: Es una especialidad de la Biología que se ocupa de establecer los diferentes taxones.
• Sistemática: Es una especialidad de la Biología que se ocupa de agrupar los diferentes taxones jerárquicamente de la forma que se considere más lógica. Actualmente se considera que lo mejor es agrupar juntos los taxones que tienen antepasados comunes.
• Nomenclatura binomial: Es una forma de denominar a cada una de las especies mediante dos nombres en latin: el primer nombre es el nombre del Género y el segundo nombre es el nombre de la especie. El nombre del Género y de la especie se han de escribir en letra cursiva si es trata de un escrito a máquina y subrayado si se trata de un manuscrito. Estos dos nombres se han de escribir siemte en minúsculas excepto la primera letra del Género que se ha de escribir con mayúscula. Por ejemplo el nombre científico del lobo se escribe así: Canis lupus (El Género es Canis y la especie es lupus).
La clasificación de los cinco reinos: Es la clasificación actual. El criterio seguido ha sido agrupar juntas las especies que tienen antepasados comunes (parentesco evolutivo).
- El primer criterio que se considera es si las células poseen núcleo (eucariotas) o no (procariotas)
- El segundo criterio que se tiene en cuenta es si son unicelulares o pluricelulares.
- El tercer criterio que se considera es si sus células forman tejidos (seres tisulares) o no (seres talofíticos).
- El cuartos criterio que se tiene en cuenta es si se alimentan de materia inorgánica (seres autótrofos) mediante la fotosíntesis o de materia orgánica (seres heterótrofos) mediante su digestión
- El quinto criterio que se considera es si la digestión la realizan segregando jugos digestivos al exterior (digestión externa) o a una cavidad o tubo digestivo interior (digestión interna).
LA CLASIFICACIÓN DE LOS 5 REINOS | Tipos de celulas | Unicelulares o Pluricelulares y talofiticos o tisulares | Tipos de nutrición | Tipo de digestión | |
1 . REINO MONERAS (Bacterias) | Procariotas | Unicelulares | Autótrofos o Heterótrofos | Externa | |
2 . REINO PROTOCTISTAS | Protozoos | Eucariotas | Unicelulares | Heteròtrofos | Interna |
Algas | Eucariotas | Unicelulares o Pluricelulares talofiticos | Autótrofos fotosintéticos | . | |
3 . REINO HONGOS | Eucariotas | Unicelulares o Pluricelulares talofiticos | Heterótrofos | Externa | |
4 . REINO METÁFITAS (PLANTAS) | Eucariotas | Pluricelulares tisulares | Autótrofos fotosintéticos | . | |
5 . REINO METAZOOS (ANIMALES) | Eucariotas | Pluricelulares tisulares | Heterótrofos | Interna | |

Muy Buen trabajo, me gusta mucho el diseño y tiene temas muy interesantes.
ResponderEliminarBuen trabajo
Me parece un trabajo exclente, muy organizado, me gusta el desarrollo por casos, cada uno con su nombre real. Es agradable en general. flicitaciones
ResponderEliminarlos temas son bastante aportantes, el diseño me gusto, felicitaciones
ResponderEliminarme parecio muy interesante tu blog, sigue asi, muy sencillo pero completo. felicitaciones.
ResponderEliminarMe perece un excelente trabajo son temas bastante importantes, sus colores muy llamativos.
ResponderEliminarBuen trabajo.
Esta muy completa la información y de forma facil de comprender, se nota un gran trabajo.
ResponderEliminarMuy interesante todos los temas publicados con mucha informacion que le aportaban a los casos! Excelentes videos e imagenes! Se nota la dedicacion! FELICITACIONES! :)
ResponderEliminarLos contenidos están muy completos, además hay mucha información, bueno que te hayas basado en los temas vistos en cada caso y que pongas la fuente pues le da más confianza al lector. Complementas la información muy bien con videos e imágenes. Felicitaciones.
ResponderEliminarMuy buen trabajo esta muy organizada la información por los casos y el diseño esta bien felicitaciones por tu trabajo
ResponderEliminarMuy buen trabajo, tienes temas muy completos y estan respaldados con imagenes y videos, lo cual lo hace mas interesante. SIGUE ASI!!!
ResponderEliminarExcelente tu blog, la información esta muy bien organizada y complementada con vídeos e imágenes, que ayudan a un mejor entendimiento, incluso mas que el mismo texto. Tu diseño es interesante, ni muy cargado ni muy sencillo, te felicito por tu trabajo y te sugeriría que miraras y fijaras bien el tamaño de las imágenes, de resto, vas muy bien
ResponderEliminarme gusta tu blog pues tiene informacion muy util complementada con imagenes y videos muy interesantes :)
ResponderEliminarEl blog es muy bueno. La información es clara y organizada, las imágenes y vídeos son precisos y acordes a los temas. Te felicito!
ResponderEliminarMuy organizado, un bonito diseño, informacion muy interesante... Felicitaciones
ResponderEliminarMuy agradable tu blog llamativo informacion muy completa se nota el trabajo muy organizado.felicitaciones.
ResponderEliminarUn blog muy organizado, agradable a la vista con información adecuada e interesante..BUEN TRABAJO!
ResponderEliminarUn muy buen blog, con informacion muy organizada, completa, ademas de tener gran cantidad de material didactico q ayuda mucho a la lectura y compresion del mismo, excelent blog. Felicitaciones!!
ResponderEliminarUno de los aspectos más importantes que se debe tener en cuenta al momento de crear un blog es el orden y tú cuentas con él en este blog. Felicitaciones, el orden de tú blog permite una clara lectura y comprensión de los temas.
ResponderEliminarlos temas se encuentran bien distribuidos!, abarcas el caso de manera completa, esto contribuye a tu aprendizaje, y los videos complementan perfectamente a la información, es bueno que siempre citas las fuentes de lo que escribes!
ResponderEliminarEste blog es de los mejores que he visto, esta muy organizado, un diseño fresco y agradable, con temas de gran interes y muy bien repartidos, muy buen trabajo
ResponderEliminarMe parece un trabajo exclente, muy organizado, me gusta el desarrollo por casos, cada uno con su nombre real y sobre todo la estetica del blog es muy interesante me gusto los colores
ResponderEliminarMe gustan los temas el orden y el diseño del blog. Felicitaciones!
ResponderEliminarexcelente trabajo te felicito por los temas, por el diseño y por tu esfuerzo en realizar este blog, espero que sigas asi
ResponderEliminartienes un blog muy bueno.. la organizacion por casos lo hace aun mas interesante.. se nota la dedicacion.. sigue trabajando vas muy bien
ResponderEliminarExcelente el orden del blog, y la informacion es demasaiada completa. Me gusta mucho el blog, al igual que la letra las imagenes son muy buenas.
ResponderEliminarme gusta mucho tu blog pq utilizas muchas tablas, videos, imagenes y para mi son mas importantes que el texto la organizacion y la estetica de tu blog es muy buena
ResponderEliminar